A análise de um hemograma inclui a leitura das três séries celulares do sangue, quais sejam, os valores quantitativos dos eritrócitos, leucócitos e plaquetas, de seus índices e as observações de suas morfologias. Além dessas informações técnicas há influências relativas às pessoas analisadas, com destaques para idades e situações clínicas associadas. Especificamente para os processos infecciosos, as análises do hemograma estão intimamente associadas às suas causas, conforme os três exemplos selecionados a seguir:
1) Infecções parasitárias, com destaque para os plasmódios da malária, quer sejam P. vivax ou P. falciparum. As alterações mais evidentes no hemograma e decisivas para o diagnóstico médico desses agentes patogênicos estão restritas notadamente aos eritrócitos. Essas células são sumariamente induzidas à morte precoce pelos parasitas que as atacam, resultando, consequentemente, em anemia hemolítica de variáveis graus entre o moderado e o acentuado, geralmente associados à reticulocitose. Morfologicamente observam-se as presenças de esferócitos, eritrócitos com policromasia, alguns, inclusive, contendo parasitas em diferentes fases de suas evoluções. A presença de parasitas intraeritrocitários é decisivo para o diagnóstico médico. Alterações leucocitárias e plaquetárias diretamente associadas às essas infecções são muito raras. Por outro lado, as infecções parasitárias por leishmanias contagiam a medula óssea, fígado e linfonodos. Especialmente na medula óssea, as leishmanias se apresentam em expressiva quantidade e interferem no desenvolvimento da hematogênese, causando leucopenia com neutropenia além da anemia e plaquetopenia. Por fim, as infecções parasitárias intestinais, crônicas e cumulativas, são causas de anemia ferropriva com variados graus de intensidades, leucocitoses discretas a moderadas às custas de eosinofilias, e também plaquetoses. Pesquisas científicas mostram que as lesões na mucosa intestinais quando extensas exigem ações contínuas de hemostasia e coagulação em focos de infeções disseminados ao longo do trato intestinal afetado. Plaquetas são estimuladas a serem produzidas e também são consumidas na hemostasia primária, e na sequência, ocorre a coagulação do sangue e a fibrinólise nos focos dessas infecções. Eosinófilos são estimulados a serem produzidos para participarem, juntamente com monócitos, da fagocitose dos restos de fibrina oriundos da fibrinólise. Dessa forma, justificam-se as plaquetoses não muito intensas e as eosinofilias que podem chegar a 50% dos leucócitos em alguns casos.
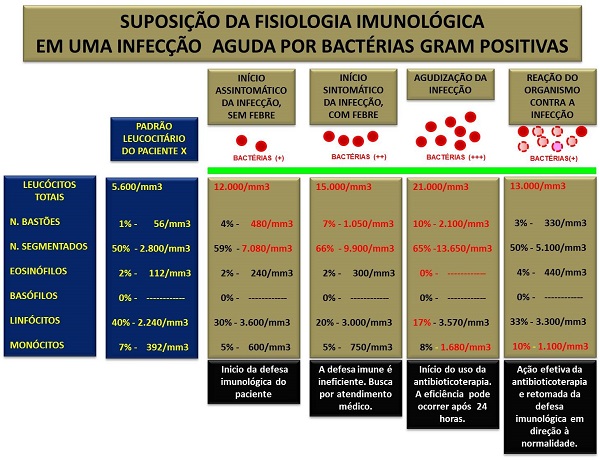
2) Infecções bacterianas, inicialmente serão dados destaques àquelas causadas por bactérias gram positivas (estreptococos piogenes e pneumonia, estafilococos aureos, micobacterias, corinebacteria difteria, etc.). Esses patógenos induzem, na maioria das vezes, as leucocitoses agudas motivadas por aumento do número de neutrófilos em valores relativos (%) e absolutos (/mm3). Dependendo da gravidade da infecção, a medula se torna hiperplásica para a linhagem de neutrófilos e libera neutrófilos segmentados, ou maduros, em grandes concentrações. Caso as bactérias infectantes apresentam-se resistentes às defesas imunológicas do paciente, a maioria dos neutrófilos maduros circulantes morrem naturalmente, pois seu tempo de vida média é curto (oito horas a quatro dias), ou nas ações antibacterianas. Nessas situações, a medula óssea libera o seu estoque de neutrófilos maduros, quase se esgotando dessas células. Na vigência da continuidade da infecção deste exemplo, a medula óssea passa a liberar grandes contingentes de neutrófilos jovens, notadamente os bastões. A presença de neutrófilos bastões em número superior ao da normalidade é denominada por desvio à esquerda. Nos estados clínicos de infecções resistentes às defesas imunológicas, a medula óssea pode, inclusive, liberar neutrófilos ainda mais jovens, como os metamielócitos e mielócitos. Na fase aguda da infecção os macrófagos passam a participarem da fagocitose das bactérias agressoras e, por conta disso, emitem intensas sinalizações biológicas através de interleucinas (IL-1 e IL-3). Essas sinalizações exercem pressões descontroladas nas células progenitoras, ou células tronco, da linhagem granulocítica de neutrófilos, fato conhecido por estresse medular. O reflexo mais evidente desse estresse é a diminuição da produção de eosinófilos e a consequente diminuição da sua liberação para o sangue periférico. Por essa razão pode ocorrer a ausência desta célula na contagem específica de 100 a 200 leucócitos. Assim, a ausência de eosinófilos é quase sempre indicativa de maior gravidade clínica da infecção bacteriana. Por outro lado, infecções causadas por bactérias gram negativas (enterobactérias, neissérias, pseudômonas, ricktécias, legionelas, etc.) liberam excessivas quantidades de toxinas nos tecidos. Essas toxinas são produtos químicos que além de atraírem leucócitos (quimiotaxia positiva) para o local da infeção, promovem, também, um afrouxamento da matriz extracelular (tecido conjuntivo, fibroblastos, adipócitos e células endoteliais) que facilita ainda mais o deslocamento de neutrófilos do sangue circulante para o foco infeccioso. Portanto, nessas infecções por bactérias gram negativas não é incomum a ocorrência de contagens diminuídas de leucócitos ou leucopenias, associadas, inclusive, com desvio à esquerda em valores relativos. Um fato importante que deve ser salientado são as mudanças radicais dos valores leucocitários em menos de 24 horas da vigência de alguns estados infecciosos por bactérias, quer sejam gram positiva ou gram negativa. Há situações de infecções por bacterias gram positivas que valores de 30 mil leucócitos diminuem abruptamente para 8 mil leucócitos num intervalo de, por exemplo, dez horas. Fatos assim podem ocorrem por intervenção terapêutica (antibioticoterapia) ou por esgotamento das reservas leucocitárias – neste caso um mal sinal de prognóstico da doença. Da mesma forma, nas infecções por bactérias gram negativas, com leucopenia e neutropenia, esses valores podem alterar de leucopenia para discretas leucocitoses, após intervenção terapêutica. Por fim, as avaliações morfológicas principalmente de neutrófilos, com destaques principalmente para as granulações tóxicas e vacuolizações, devem ser relatadas, inclusive com avaliações semi-quantitativas, pois suas presenças podem estar relacionadas ações de bactérias supurativas, entre outras causas. A figura abaixo resume uma suposição fisiológica das fases de uma infecção bacteriana aguda relacionada com variações numéricas do leucograma.
3) Infecções virais, inicialmente destacarei o vírus da influenza ou da gripe, as famosas viroses. Esse vírus apresentam facilidades de mutações e infectam continuadamente as populações humanas, entre outras. Quando as infecções virais estão associadas à febre, tremores e calafrios é possível observar no hemograma a presença de leucocitose, com valores aumentados de linfócitos (relativo e absoluto). Excetuando essas situações, é mais comum a contagem diminuída de leucócitos (geralmente por volta de 2.500 a 3.500/mm3), com valores de linfócitos superiores a 50%. Entretanto, é possível que pessoas infectadas por esses vírus se apresentam com resultados normais para leucócitos, porém, associados à linfocitose relativa. Outros tipos de infecções virais de importância se devem aos vírus da dengue (DEN-1, DEN-2, DEN-3 e DEN-4) e da chikungunya (CHIKV). Ambos causam manifestações de doenças clinicamente parecidas com evolução em três fases: aguda, subaguda e crônica. Há testes diferenciais para seus diagnósticos e acompanhamento clínico, mas o hemograma é o exame mais solicitado e de muita utilidade no acompanhamento da doença. Nas duas doenças ocorrem: plaquetopenia, leucopenia e neutropenia, todas essas alterações são maiores na dengue do que na chikungunya. Somente a linfopenia (<1000/mm3) é maior na chikungunya do que na dengue. Nas infecções virais, de uma forma geral, as avaliações morfológicas dos linfócitos são muito importantes, principalmente na constatação dos linfócitos atípicos, o que significa um bom sinal de resistência imunológica. Os linfócitos atípicos se caracterizam por alterações de conteúdo (linfócitos B carregados com anticorpos contra os vírus agressores), ou de receptores de membrana (linfócitos T CD4 e CD8) que reagem intensamente com fatores de indução de sinalização. Os linfócitos atípicos geralmente são maiores que os linfócitos normais, apresentam-se com aumento do volume citoplasmático e são mais basofílicos. A maioria das pessoas saudáveis tem linfócitos atípicos motivados por infecções virais sintomáticas ou assintomática que as afetam continuadamente. Pesquisas relatam que pessoas saudáveis tem até 5% de linfócitos atípicos entre o total de leucócitos contabilizados. Por essa razão, suas presenças devem ser anotadas apenas quando o número dessas células superarem a quantidade de 5%, especificando, assim, o valor encontrado. Outros tipos de viroses, com destaques para a mononucleose infecciosa, envolve não apenas os linfócitos, mas também os monócitos. No entanto, os monócitos merecem um artigo específico, pois cada vez mais esta célula se mostra como a mais influente na nossa defesa imunológica.